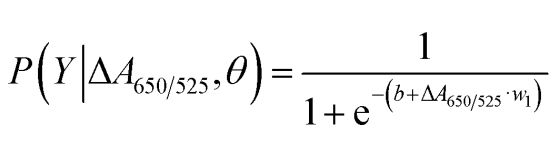A detección precoz do cancro baseada na biopsia líquida é unha nova dirección de detección e diagnóstico do cancro proposta polo Instituto Nacional do Cancro dos Estados Unidos nos últimos anos, co obxectivo de detectar cancro precoz ou mesmo lesións precancerosas. Utilizouse amplamente como un novo biomarcador para o diagnóstico precoz de diversas neoplasias malignas, incluíndo cancro de pulmón, tumores gastrointestinais, gliomas e tumores xinecolóxicos.
A aparición de plataformas para identificar biomarcadores da paisaxe da metilación (Methylscape) ten o potencial de mellorar significativamente a detección precoz do cancro, colocando aos pacientes na fase tratable máis temperá.
Recentemente, os investigadores desenvolveron unha plataforma de detección sinxela e directa para a detección de paisaxes de metilación baseada en nanopartículas de ouro decoradas con cisteamina (Cist/AuNPs) combinadas cun biosensor baseado en teléfono intelixente que permite a detección temperá e rápida dunha ampla gama de tumores. A detección temperá da leucemia pódese realizar nos 15 minutos posteriores á extracción de ADN dunha mostra de sangue, cunha precisión do 90,0 %. O título do artigo é Detección rápida de ADN canceroso en sangue humano usando AuNPs cubertas con cisteamina e un teléfono intelixente con aprendizaxe automática.
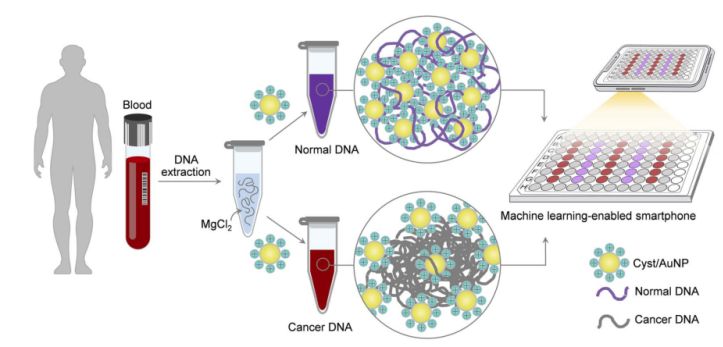
Figura 1. Unha plataforma de detección sinxela e rápida para o cribado do cancro mediante compoñentes de quiste/AuNPs pódese conseguir en dous pasos sinxelos.
Isto móstrase na Figura 1. Primeiro, utilizouse unha solución acuosa para disolver os fragmentos de ADN. Despois, engadíronse nanopartículas de ADN tipo quiste/AuNP á solución mesturada. O ADN normal e o maligno teñen diferentes propiedades de metilación, o que resulta en fragmentos de ADN con diferentes patróns de autoensamblaxe. O ADN normal agrégase de forma libre e finalmente agrega nanopartículas de ADN tipo quiste/AuNP, o que resulta na natureza desprazada cara ao vermello das nanopartículas de ADN tipo quiste/AuNP, de xeito que se pode observar a simple vista un cambio de cor de vermello a púrpura. Pola contra, o perfil único de metilación do ADN canceroso leva á produción de clústeres máis grandes de fragmentos de ADN.
Tomáronse imaxes de placas de 96 pozos coa cámara dun teléfono intelixente. O ADN canceroso mediuse cun teléfono intelixente equipado con aprendizaxe automática en comparación cos métodos baseados en espectroscopia.
Detección do cancro en mostras de sangue real
Para ampliar a utilidade da plataforma de detección, os investigadores aplicaron un sensor que distinguía con éxito entre ADN normal e canceroso en mostras de sangue real. Os patróns de metilación nos sitios CpG regulan epixeneticamente a expresión xénica. En case todos os tipos de cancro, observouse que os cambios na metilación do ADN e, polo tanto, na expresión dos xenes que promoven a tumorexénese se alternan.
Como modelo para outros cancros asociados coa metilación do ADN, os investigadores empregaron mostras de sangue de pacientes con leucemia e controis sans para investigar a eficacia da paisaxe da metilación na diferenciación dos cancros leucémicos. Este biomarcador da paisaxe da metilación non só supera os métodos de cribado rápido da leucemia existentes, senón que tamén demostra a viabilidade de estender a detección precoz dunha ampla gama de cancros mediante este ensaio sinxelo e directo.
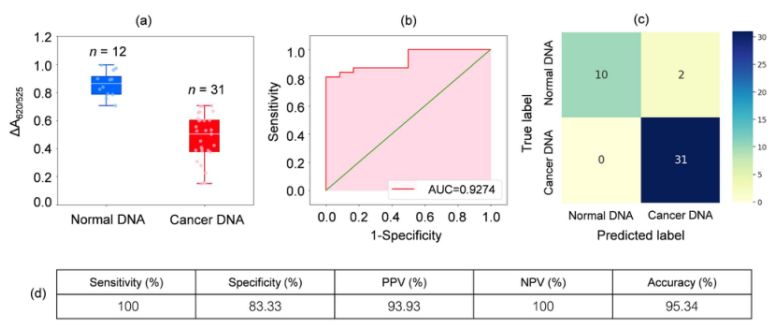
Analizouse o ADN de mostras de sangue de 31 pacientes con leucemia e 12 individuos sans. Como se mostra no diagrama de caixa da Figura 2a, a absorbancia relativa das mostras de cancro (ΔA650/525) foi menor que a do ADN de mostras normais. Isto debeuse principalmente á maior hidrofobicidade, o que levou a unha densa agregación de ADN de cancro, o que impediu a agregación de quistes/AuNPs. Como resultado, estas nanopartículas dispersáronse completamente nas capas externas dos agregados de cancro, o que resultou nunha dispersión diferente de quistes/AuNPs adsorbidas nos agregados de ADN normal e de cancro. As curvas ROC xeráronse entón variando o limiar desde un valor mínimo de ΔA650/525 ata un valor máximo.
Figura 2.(a) Valores de absorbancia relativa de solucións de quistes/AuNPs que mostran a presenza de ADN normal (azul) e canceroso (vermello) en condicións optimizadas.
(DA650/525) de diagramas de caixa; (b) Análise ROC e avaliación de probas diagnósticas. (c) Matriz de confusión para o diagnóstico de pacientes normais e con cancro. (d) Sensibilidade, especificidade, valor preditivo positivo (VPP), valor preditivo negativo (VPN) e precisión do método desenvolvido.
Como se mostra na Figura 2b, a área baixo a curva ROC (AUC = 0,9274) obtida para o sensor desenvolvido mostrou alta sensibilidade e especificidade. Como se pode ver no diagrama de caixa, o punto máis baixo que representa o grupo de ADN normal non está ben separado do punto máis alto que representa o grupo de ADN canceroso; polo tanto, utilizouse a regresión loxística para diferenciar entre os grupos normal e canceroso. Dado un conxunto de variables independentes, estima a probabilidade de que ocorra un evento, como un grupo canceroso ou normal. A variable dependente oscila entre 0 e 1. Polo tanto, o resultado é unha probabilidade. Determinamos a probabilidade de identificación do cancro (P) baseándonos en ΔA650/525 do seguinte xeito.
onde b=5,3533,w1=-6,965. Para a clasificación da mostra, unha probabilidade inferior a 0,5 indica unha mostra normal, mentres que unha probabilidade de 0,5 ou superior indica unha mostra de cancro. A figura 2c representa a matriz de confusión xerada a partir da validación cruzada de tipo "leave-it-alone", que se empregou para validar a estabilidade do método de clasificación. A figura 2d resume a avaliación da proba diagnóstica do método, incluíndo a sensibilidade, a especificidade, o valor preditivo positivo (VPP) e o valor preditivo negativo (VPN).
Biosensores baseados en teléfonos intelixentes
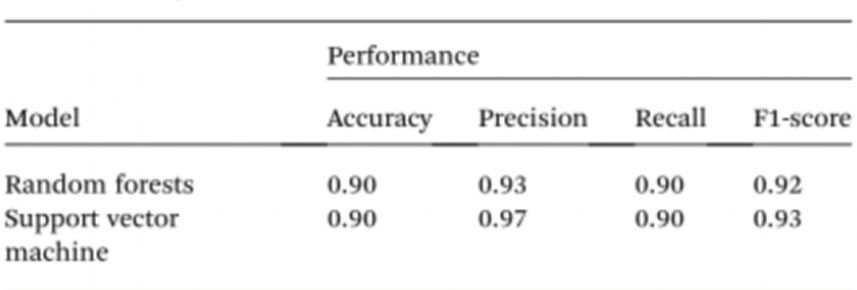
Para simplificar aínda máis as análises de mostras sen o uso de espectrofotómetros, os investigadores empregaron a intelixencia artificial (IA) para interpretar a cor da solución e distinguir entre individuos normais e cancerosos. Tendo isto en conta, empregouse a visión artificial para traducir a cor da solución de quistes/AuNPs a ADN normal (púrpura) ou ADN canceroso (vermello) utilizando imaxes de placas de 96 pozos tomadas a través da cámara dun teléfono móbil. A intelixencia artificial pode reducir os custos e mellorar a accesibilidade na interpretación da cor das solucións de nanopartículas, e sen o uso de ningún accesorio de hardware óptico para teléfonos intelixentes. Finalmente, adestráronse dous modelos de aprendizaxe automática, incluíndo Random Forest (RF) e Support Vector Machine (SVM), para construír os modelos. Tanto o modelo RF como o SVM clasificaron correctamente as mostras como positivas e negativas cunha precisión do 90,0 %. Isto suxire que o uso da intelixencia artificial na biosensoría baseada en teléfonos móbiles é bastante posible.
Figura 3.(a) Clase obxectivo da solución rexistrada durante a preparación da mostra para o paso de adquisición da imaxe. (b) Imaxe de exemplo tomada durante o paso de adquisición da imaxe. (c) Intensidade da cor da solución de quiste/AuNPs en cada pozo da placa de 96 pozos extraída da imaxe (b).
Usando Cyst/AuNPs, os investigadores desenvolveron con éxito unha plataforma de detección sinxela para a detección de paisaxes de metilación e un sensor capaz de distinguir o ADN normal do ADN canceroso ao usar mostras de sangue real para o cribado de leucemia. O sensor desenvolvido demostrou que o ADN extraído de mostras de sangue real era capaz de detectar de forma rápida e rendible pequenas cantidades de ADN canceroso (3 nM) en pacientes con leucemia en 15 minutos, e mostrou unha precisión do 95,3 %. Para simplificar aínda máis as probas de mostras ao eliminar a necesidade dun espectrofotómetro, utilizouse a aprendizaxe automática para interpretar a cor da solución e diferenciar entre individuos normais e cancerosos mediante unha fotografía de teléfono móbil, e tamén se puido alcanzar unha precisión do 90,0 %.
Referencia: DOI: 10.1039/d2ra05725e
Data de publicación: 18 de febreiro de 2023
 中文网站
中文网站