Nat Med | Unha abordaxe multiómica para mapear a paisaxe integrada tumoral, inmunolóxica e microbiana do cancro colorrectal revela a interacción do microbioma co sistema inmunitario
Aínda que os biomarcadores do cancro de colon primario foron estudados amplamente nos últimos anos, as guías clínicas actuais baséanse só na estadificación tumor-ganglio linfático-metástase e na detección de defectos de reparación de erros de emparellamento do ADN (MMR) ou inestabilidade de microsatélites (MSI) (ademais das probas patolóxicas estándar) para determinar as recomendacións de tratamento. Os investigadores observaron unha falta de asociación entre as respostas inmunitarias baseadas na expresión xénica, os perfís microbianos e o estroma tumoral na cohorte de cancro colorrectal do Atlas do Xenoma do Cancro (TCGA) e a supervivencia dos pacientes.
A medida que a investigación foi avanzando, informouse de que as características cuantitativas do cancro colorrectal primario, incluída a natureza celular, inmunitaria, estromal ou microbiana do cancro, se correlacionan significativamente cos resultados clínicos, pero aínda hai unha comprensión limitada de como as súas interaccións afectan aos resultados dos pacientes.
Para analizar a relación entre a complexidade fenotípica e o resultado, un equipo de investigadores do Instituto Sidra de Investigación Médica de Qatar desenvolveu e validou recentemente unha puntuación integrada (mICRoScore) que identifica un grupo de pacientes con boas taxas de supervivencia combinando as características do microbioma e as constantes de rexeitamento inmunitario (ICR). O equipo realizou unha análise xenómica exhaustiva de mostras conxeladas frescas de 348 pacientes con cancro colorrectal primario, incluíndo a secuenciación do ARN de tumores e tecido colorrectal san correspondente, a secuenciación do exoma completo, a secuenciación profunda do receptor de células T e o xene do ARNr bacteriano 16S, complementada coa secuenciación do xenoma tumoral completo para caracterizar aínda máis o microbioma. O estudo publicouse en Nature Medicine como "Un atlas integrado de tumores, inmunitario e microbioma do cancro de colon".

Artigo publicado en Nature Medicine
Visión xeral de AC-ICAM
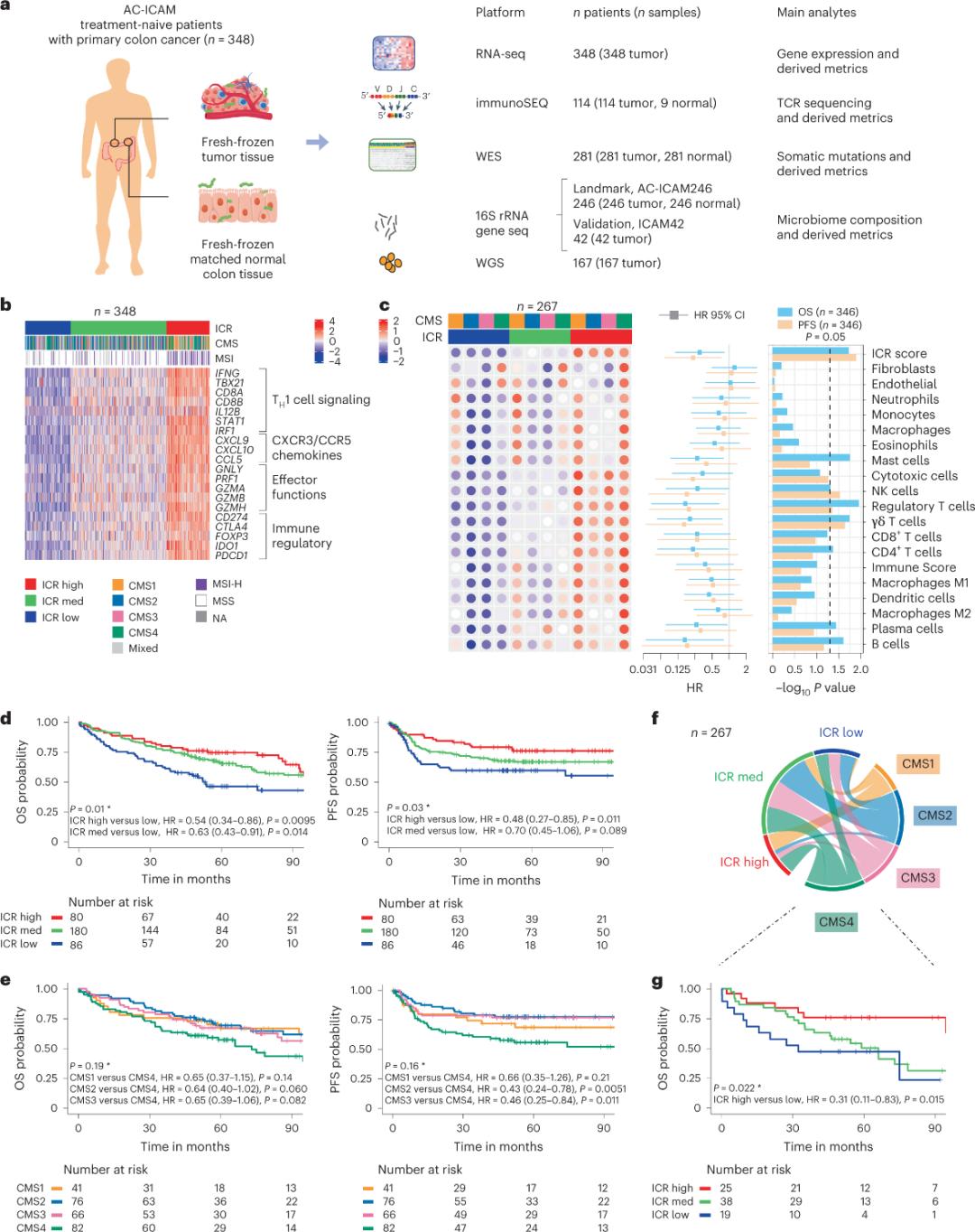
Os investigadores empregaron unha plataforma xenómica ortogonal para analizar mostras tumorais frescas conxeladas e emparellaron tecido de colon san adxacente (pares tumor-normal) de pacientes cun diagnóstico histolóxico de cancro de colon sen terapia sistémica. Baseándose na secuenciación do exoma completo (WES), o control de calidade dos datos de RNA-seq e a selección de criterios de inclusión, retiráronse datos xenómicos de 348 pacientes e utilizáronse para análises posteriores cunha mediana de seguimento de 4,6 anos. O equipo de investigación denominou este recurso Sidra-LUMC AC-ICAM: Un mapa e unha guía das interaccións inmuno-cancer-microbioma (Figura 1).
Clasificación molecular mediante ICR
Ao capturar un conxunto modular de marcadores xenéticos inmunitarios para a inmunovixilancia continua do cancro, denominado constante inmunitaria de rexeitamento (ICR), o equipo de investigación optimizou a ICR condensándoa nun panel de 20 xenes que abrangue diferentes tipos de cancro, incluíndo melanoma, cancro de vexiga e cancro de mama. A ICR tamén se asociou coa resposta á inmunoterapia nunha variedade de tipos de cancro, incluído o cancro de mama.
En primeiro lugar, os investigadores validaron a sinatura ICR da cohorte AC-ICAM, empregando unha abordaxe de coclasificación baseada en xenes ICR para clasificar a cohorte en tres grupos/subtipos inmunitarios: ICR alta (tumores quentes), ICR media e ICR baixa (tumores fríos) (Figura 1b). Os investigadores caracterizaron a propensión inmunitaria asociada aos subtipos moleculares de consenso (CMS), unha clasificación do cancro de colon baseada no transcriptoma. As categorías CMS incluían CMS1/inmune, CMS2/canónico, CMS3/metabólico e CMS4/mesenquimal. A análise mostrou que as puntuacións ICR estaban correlacionadas negativamente con certas vías das células cancerosas en todos os subtipos CMS, e observáronse correlacións positivas con vías inmunosupresoras e relacionadas co estroma só nos tumores CMS4.
En todos os CMS, a abundancia de subconxuntos de células asasinas naturais (NK) e células T foi maior nos subtipos de ICR inmunitario alto, con maior variabilidade noutros subconxuntos de leucocitos (Figura 1c). Os subtipos inmunitarios de ICR tiveron diferente OS e PFS, cun aumento progresivo da ICR de baixa a alta (Figura 1d), o que valida o papel pronóstico da ICR no cancro colorrectal.
Figura 1. Deseño do estudo AC-ICAM, sinatura xénica relacionada co sistema inmunitario, subtipos inmunitarios e moleculares e supervivencia.
A ICR captura células T amplificadas clonalmente e enriquecidas con tumores
Só se informou de que unha minoría de linfocitos T que se infiltran no tecido tumoral son específicos para antíxenos tumorais (menos do 10 %). Polo tanto, a maioría dos linfocitos T intratumorais denomínanse linfocitos T espectadores (células T espectadoras). A correlación máis forte co número de linfocitos T convencionais con TCR produtivos observouse nas subpoboacións de células estromais e leucocitos (detectados por RNA-seq), que se poden usar para estimar as subpoboacións de linfocitos T (Figura 2a). Nos clústeres de ICR (clasificación xeral e CMS), a maior clonalidade dos TCR de SEC inmunitaria observouse nos grupos CMS1/inmune con ICR alto e subtipo CMS (Figura 2c), coa maior proporción de tumores con ICR alto. Usando o transcriptoma completo (18 270 xenes), seis xenes ICR (IFNG, STAT1, IRF1, CCL5, GZMA e CXCL10) estaban entre os dez principais xenes asociados positivamente coa clonalidade da SEC inmunitaria do TCR (Figura 2d). A clonalidade do TCR de ImmunoSEQ correlacionouse máis fortemente coa maioría dos xenes ICR que as correlacións observadas usando marcadores CD8+ sensibles a tumores (Figura 2f e 2g). En conclusión, a análise anterior suxire que a sinatura ICR captura a presenza de células T amplificadas clonalmente e enriquecidas con tumores, e pode explicar as súas implicacións prognósticas.
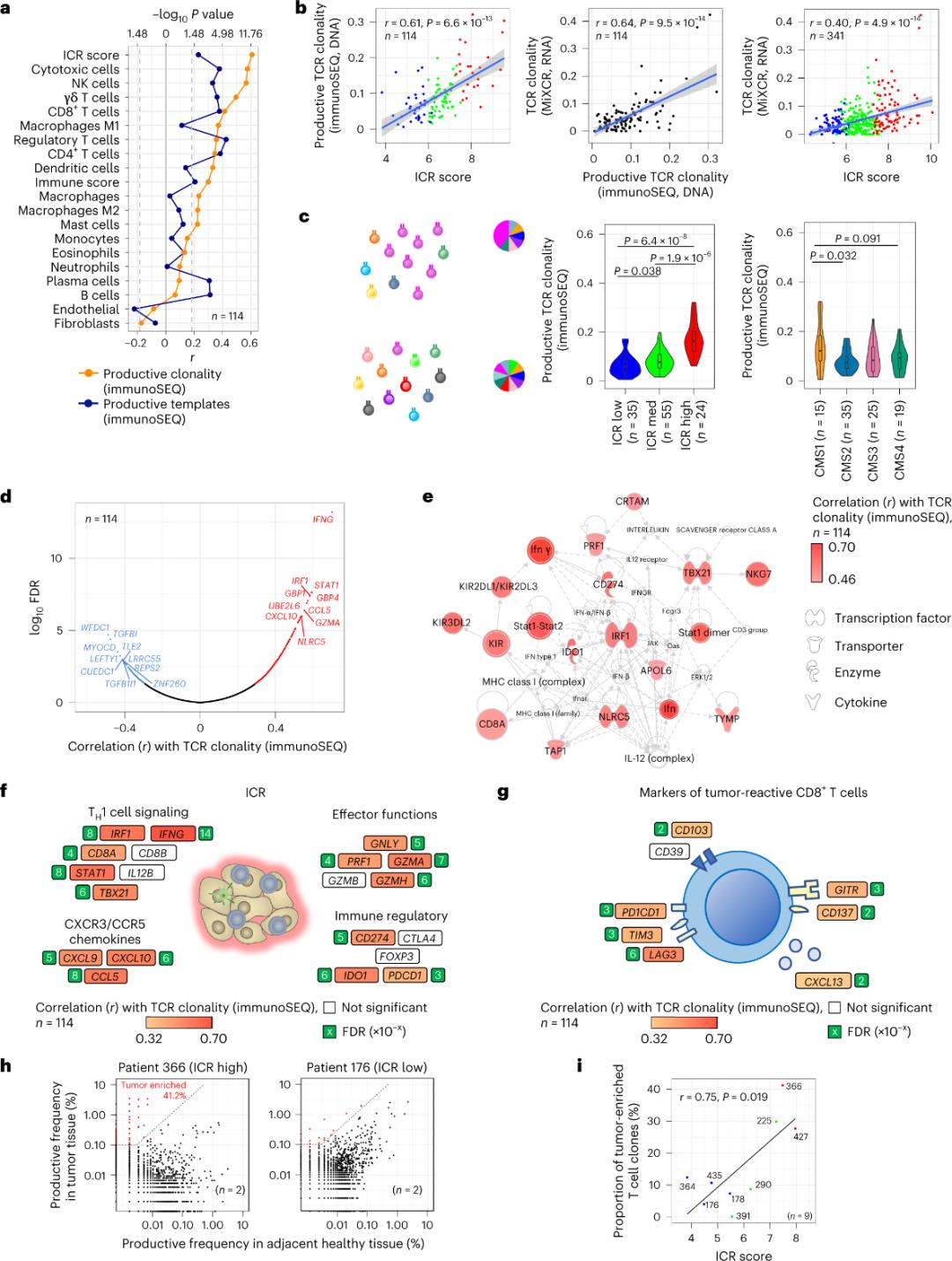
Figura 2. Métricas do TCR e correlación con xenes relacionados co sistema inmunitario, subtipos inmunitarios e moleculares.
Composición do microbioma en tecidos sans e cancerosos de colon
Os investigadores realizaron a secuenciación do ARNr 16S empregando ADN extraído de tecido tumoral e de colon san emparellados de 246 pacientes (Figura 3a). Para a validación, os investigadores analizaron adicionalmente os datos de secuenciación do xene do ARNr 16S doutras 42 mostras tumorais que non tiñan ADN normal coincidente dispoñible para a análise. En primeiro lugar, os investigadores compararon a abundancia relativa de flora entre os tumores emparellados e o tecido colon san. O *Clostridium perfringens* aumentou significativamente nos tumores en comparación coas mostras sas (Figuras 3a-3d). Non houbo diferenzas significativas na diversidade alfa (diversidade e abundancia de especies nunha soa mostra) entre as mostras tumorais e as sas, e observouse unha modesta redución da diversidade microbiana nos tumores con ICR alto en relación cos tumores con ICR baixo.
Para detectar asociacións clinicamente relevantes entre os perfís microbianos e os resultados clínicos, os investigadores tiveron como obxectivo usar datos de secuenciación do xene ARNr 16S para identificar as características do microbioma que predicen a supervivencia. No AC-ICAM246, os investigadores executaron un modelo de regresión OS Cox que seleccionou 41 características con coeficientes distintos de cero (asociadas ao risco de mortalidade diferencial), chamadas clasificadores MBR (Figura 3f).
Nesta cohorte de adestramento (ICAM246), unha puntuación MBR baixa (MBR < 0, MBR baixa) asociouse cun risco significativamente menor de morte (85%). Os investigadores confirmaron a asociación entre unha MBR baixa (risco) e unha SG prolongada en dúas cohortes validadas de forma independente (ICAM42 e TCGA-COAD). (Figura 3). O estudo mostrou unha forte correlación entre os cocos endogástricos e as puntuacións MBR, que foron similares no tecido tumoral e no tecido colónico san.
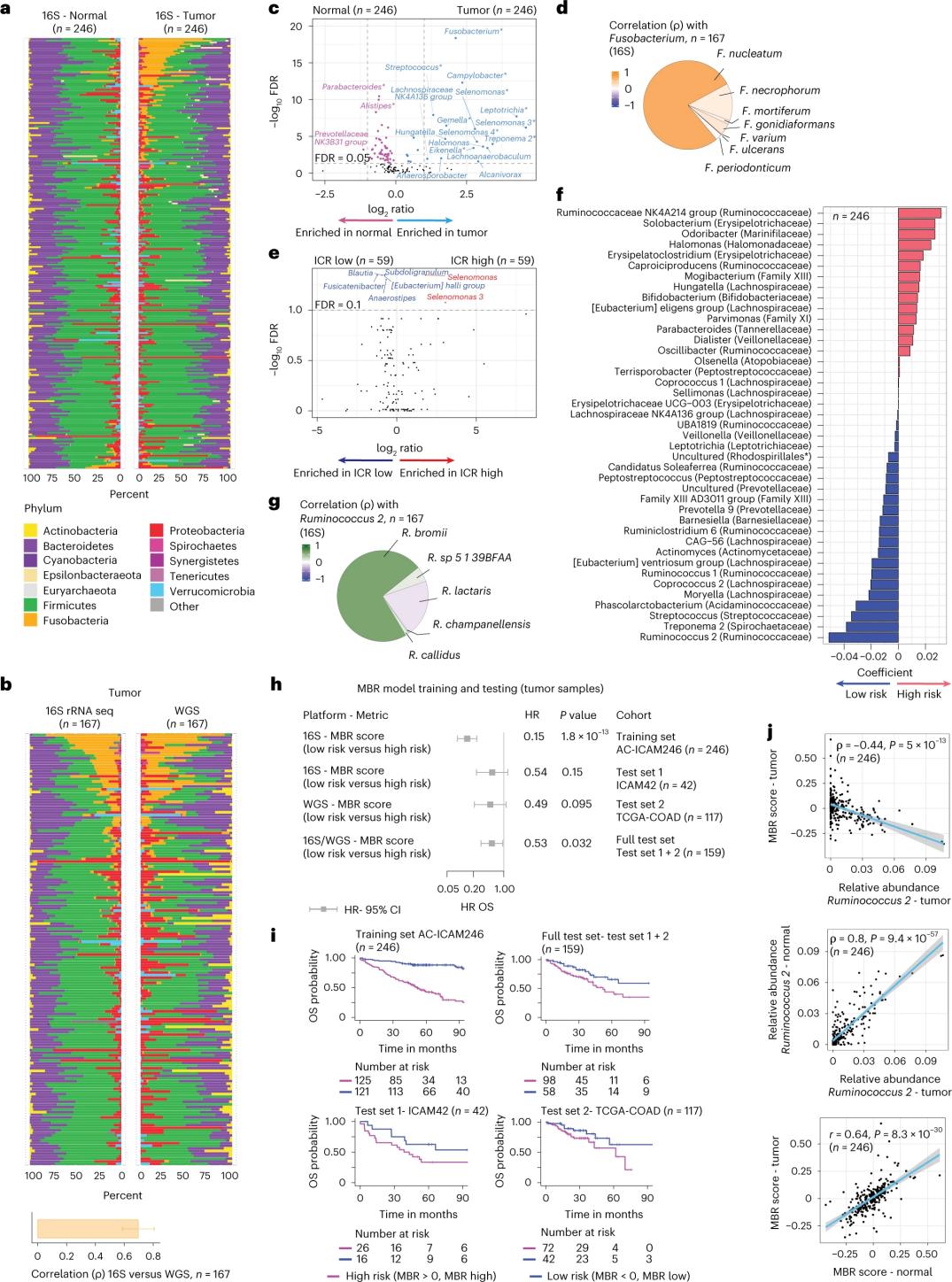
Figura 3. Microbioma en tecidos tumorais e sans e a relación coa ICR e a supervivencia do paciente.
Conclusión
A abordaxe multiómica empregada neste estudo permite a detección e análise exhaustivas da sinatura molecular da resposta inmunitaria no cancro colorrectal e revela a interacción entre o microbioma e o sistema inmunitario. A secuenciación profunda do TCR de tecidos tumorais e sans revelou que o efecto prognóstico da ICR pode deberse á súa capacidade para capturar clons de células T enriquecidas con tumores e posiblemente específicas de antíxenos tumorais.
Ao analizar a composición do microbioma tumoral mediante a secuenciación do xene 16S rRNA en mostras AC-ICAM, o equipo identificou unha sinatura do microbioma (puntuación de risco MBR) cun forte valor prognóstico. Aínda que esta sinatura se derivou de mostras tumorais, houbo unha forte correlación entre o colorrecto san e a puntuación de risco MBR tumoral, o que suxire que esta sinatura pode capturar a composición do microbioma intestinal dos pacientes. Ao combinar as puntuacións ICR e MBR, foi posible identificar e validar un biomarcador multiómico de Student que predí a supervivencia en pacientes con cancro de colon. O conxunto de datos multiómicos do estudo proporciona un recurso para comprender mellor a bioloxía do cancro de colon e axudar a descubrir enfoques terapéuticos personalizados.
Data de publicación: 15 de xuño de 2023
 中文网站
中文网站